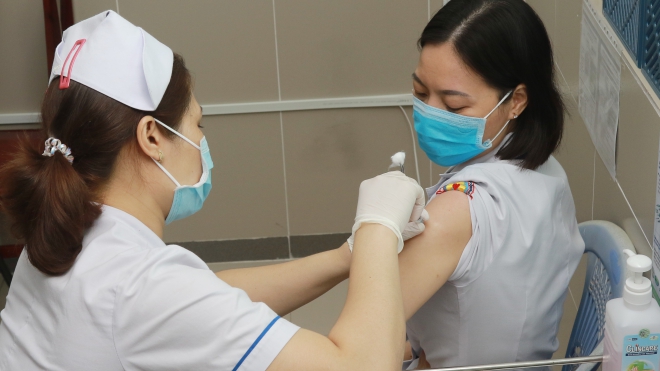
Dịch Covid-19: Pfizer/BioNTech đề nghị cấp phép sử dụng đối với vaccine dành cho trẻ 12-15 tuổi
10/04/2021 13:58 GMT+7 | Thế giới
(giaidauscholar.com) - Ngày 9/4, hai hãng dược phẩm Pfizer (Mỹ) và BioNTech (Đức) đã đề nghị Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) cấp phép sử dụng khẩn cấp đối với vaccine của hai hãng này với đối tượng trẻ em từ 12-15 tuổi tại Mỹ, động thái đánh dấu bước đi quan trọng nhằm đạt được miễn dịch cộng đồng.
Hiện, các nhà quản lý mới cấp phép sử dụng khẩn cấp vaccine của Pfizer/BioNTech cho người từ 16 tuổi trở lên tại Mỹ. Trong một tuyên bố, Pfizer/BioNTech cũng cho biết họ có kế hoạch đưa ra đề nghị tương tự đối với các cơ quan quản lý khác trên khắp thế giới trong những ngày tới.
Trước đó, trong báo cáo công bố hồi tháng 3, Pfizer/BioNTech khẳng định trong giai đoan 3 thử nghiệm lâm sàng, vaccine do hai hãng phối hợp bào chế đã chứng tỏ hiệu quả 100% trong việc phòng ngừa virus SARS-CoV-2 đối với trẻ em từ 12-15 tuổi và tạo kháng thể mạnh.
- Có 8 tỉnh, thành phố đã hoàn thành đợt 1 tiêm vaccine phòng COVID-19
- Dịch Covid-19: Bộ Y tế nêu ý kiến về phương án 'hộ chiếu vaccine'
- Dịch Covid-19: Ghi nhận 14 ca mắc mới, đều là người nhập cảnh
Hiện chưa rõ thời gian các nhà quản lý Mỹ rà soát dữ liệu trong giai đoạn thử nghiệm lâm sàng vaccine của Pfizer/BioNTech, song trong trả lời phỏng vấn kênh ABC News ngày 8/4, Giám đốc FDA Rochelle Walensky kỳ vọng vaccine này sẽ được cấp phép sử dụng cho lứa tuổi từ 12-15 tuổi vào giữa tháng 5 tới.
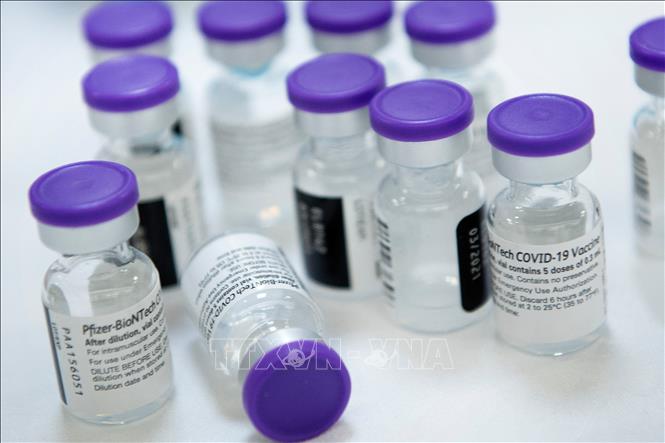
Các nhà quản lý Mỹ cho biết chưa có kế hoạch tiến hành cuộc họp của một ủy ban cố vấn độc lập nhằm xem xét việc cấp sử dụng đối với vaccine cho giai đoạn tuổi trên. Trong khi đó, vaccine ngừa COVID-19 của hai hãng Moderna và Johnson & Johnson được FDA cấp phép sử dụng cho những người từ 18 tuổi trở lên. Pfizer và Moderna đang triển khai các cuộc thử nghiệm lầm sàng cho những đối tượng từ 6 tháng - 11 tuổi. Cả hai công ty này kỳ vọng có thể tiêm cho trẻ dưới 11 tuổi sớm nhất vào đầu năm 2022.
Các chuyên gia y tế cho biết việc tiêm vaccine ngừa COVID-19 cho trẻ em và người trẻ tuổi được xem là bước đi quan trọng giúp đạt miễn dịch cộng đồng và ngăn chặn đại dịch này.
TTXVN
-
 13/07/2025 16:59 0
13/07/2025 16:59 0 -
-
-
 13/07/2025 15:59 0
13/07/2025 15:59 0 -

-

-

-
 13/07/2025 15:46 0
13/07/2025 15:46 0 -
 13/07/2025 15:45 0
13/07/2025 15:45 0 -

-

-

-

-

-

-
-
 13/07/2025 14:14 0
13/07/2025 14:14 0 -
 13/07/2025 13:03 0
13/07/2025 13:03 0 -

-

- Xem thêm ›