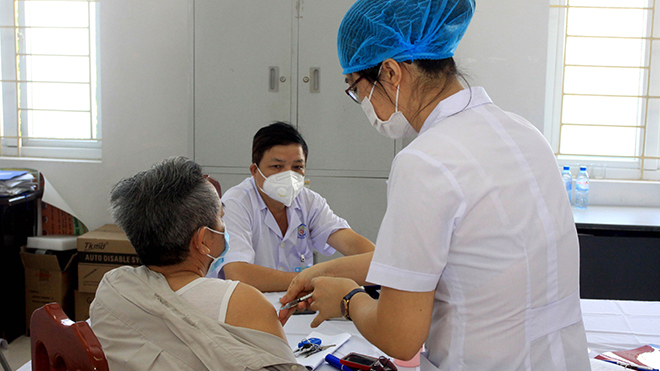
Bộ Y tế hướng dẫn đăng ký lưu hành vaccine Covid-19 trong trường hợp cấp bách
20/08/2021 22:25 GMT+7 | Trong nước
(giaidauscholar.com) - Hướng dẫn về việc đăng ký lưu hành vaccine COVID-19 trong trường hợp cấp bách của Bộ Y tế nêu rõ: vaccine COVID-19 sản xuất trong nước đang thử nghiệm lâm sàng nhưng có kết quả đánh giá giữa kỳ giai đoạn 3 về tính an toàn và hiệu quả bảo vệ dựa trên dữ liệu về tính sinh miễn dịch được sử dụng để xem xét cấp giấy đăng ký lưu hành có điều kiện.
Theo hướng dẫn của Bộ Y tế, vaccine COVID-19 trong nước đang thử nghiệm lâm sàng được xem xét cấp giấy đăng ký lưu hành có điều kiện khi đã có kết quả đánh giá giữa kỳ giai đoạn 3 về tính an toàn và hiệu quả bảo vệ của vaccine dựa trên dữ liệu về tính sinh miễn dịch của vaccine được sử dụng để xem xét cấp giấy đăng ký lưu hành có điều kiện.
Việc này được thực hiện trên cơ sở ý kiến tư vấn của Hội đồng Đạo đức trong nghiên cứu y sinh học cấp quốc gia đối với thực hiện thử nghiệm lâm sàng tại Việt Nam và ý kiến tư vấn của Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc đối với từng vaccine cụ thể, có tham khảo hướng dẫn hoặc khuyến cáo của Tổ chức Y tế thế giới (WHO).
Bộ Y tế lưu ý, vaccine được cấp trong trường hợp trên phải được tiếp tục theo dõi về tính an toàn, hiệu quả, kiểm soát về đối tượng, số lượng, phạm vi sử dụng sau khi cấp giấy đăng ký lưu hành.
Sau khi được cấp phép lưu hành, cơ sở đăng ký phối hợp với cơ sở sản xuất tiếp tục thực hiện nghiên cứu lâm sàng và cập nhật dữ liệu lâm sàng theo hướng dẫn của Bộ Y tế (Cục Khoa học công nghệ và Đào tạo).
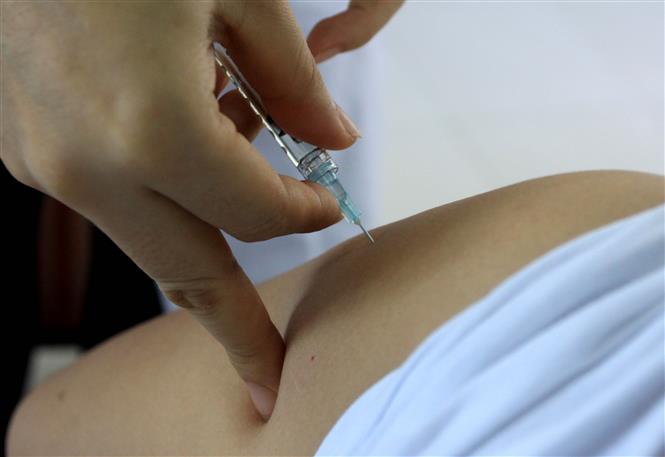
Vaccine chưa đáp ứng quy định được Bộ trưởng Bộ Y tế xem xét quyết định miễn một, một số giai đoạn thử thuốc trên lâm sàng (bao gồm cả miễn giảm dữ liệu lâm sàng) trên cơ sở ý kiến tư vấn của Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc khi thuộc một trong các trường hợp sau:
Vaccine đã được cấp phép lưu hành tại ít nhất một nước trên thế giới và có dữ liệu lâm sàng về an toàn, hiệu quả.
Trường hợp cơ quan quản lý dược của nước đã cấp phép lưu hành không thuộc một trong các cơ quan quản lý quy định tại khoản 10 Điều 2 Thông tư số 32/2018/TT-BYT, sau khi được cấp giấy đăng ký lưu hành, cơ sở đăng ký phối hợp với cơ sở sản xuất phải tiếp tục đánh giá tính an toàn và tính sinh miễn dịch trên quần thể đích tại Việt Nam trong quá trình sử dụng theo hướng dẫn của Bộ Y tế (Cục Khoa học công nghệ và Đào tạo).
Vaccine được sản xuất tại Việt Nam theo hình thức chuyển giao công nghệ một, một số hoặc toàn bộ các công đoạn của quy trình sản xuất thành phẩm mà vaccine trước chuyển giao công nghệ có dữ liệu lâm sàng về an toàn, hiệu quả đã được cấp phép lưu hành tại ít nhất một nước trên thế giới.
Trường hợp phải thử lâm sàng giai đoạn 4 tại Việt Nam hướng dẫn của Bộ Y tế nêu rõ trên cơ sở ý kiến tư vấn của Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc, vaccine đã được cấp giấy đăng ký lưu hành nhưng cần đánh giá thêm về an toàn, hiệu quả thì phải thử lâm sàng giai đoạn 4 tại Việt Nam.
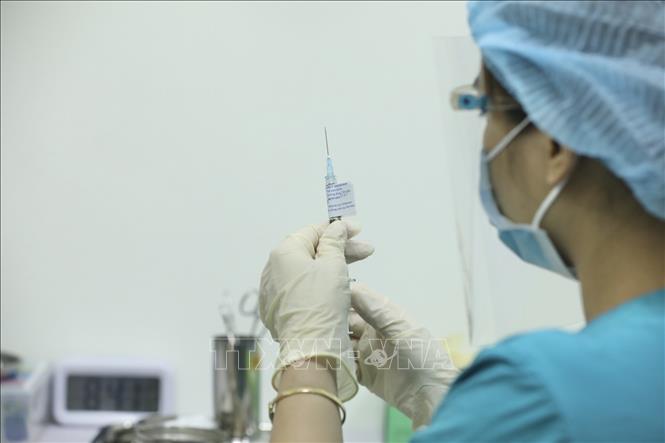
Liên quan đến thủ tục cấp giấy đăng ký lưu hành vaccine, hướng dẫn của Bộ Y tế nêu rõ: Trong thời hạn tối đa 20 ngày làm việc kể từ ngày nhận đủ hồ sơ đối với hồ sơ đề nghị cấp giấy đăng ký lưu hành vaccine, Cục trưởng Cục Quản lý dược cấp giấy đăng ký lưu hành vaccine. Trường hợp không cấp hoặc chưa cấp, Cục Quản lý dược có văn bản thông báo và nêu rõ lý do.
Sau khi có văn bản thông báo yêu cầu bổ sung của Cục Quản lý dược, trong thời hạn 36 tháng đối với trường hợp có yêu cầu bổ sung tài liệu tiền lâm sàng và lâm sàng, tài liệu nghiên cứu độ ổn định hoặc trong thời hạn 12 tháng đối với các trường hợp bổ sung tài liệu khác. Sau thời hạn này, cơ sở đăng ký không nộp tài liệu bổ sung thì hồ sơ đã nộp không còn giá trị.
- Bộ Y tế cho ý kiến về đề xuất tiêm vaccine phòng Covid-19 cho trẻ từ 12-18 tuổi
- Bộ Y tế thông tin về mở rộng địa điểm tiêm thử nghiệm giai đoạn 3 vaccine Nanocovax
- Bộ Y tế hướng dẫn khám sàng lọc trước tiêm chủng vaccine phòng Covid-19
Cơ sở đăng ký thông báo bằng văn bản về Cục Quản lý dược trường hợp có các thông tin cập nhật liên quan đến an toàn, hiệu quả của vaccine so với hồ sơ đăng ký đã nộp và đang trong thời gian thẩm định. Thời gian kể từ khi có văn bản thông báo của Cục Quản lý dược đến khi cơ sở đăng ký nộp tài liệu bổ sung không được tính vào thời hạn quy định kể trên.
Trong thời hạn 15 ngày làm việc kể từ ngày nhận đủ tài liệu bổ sung, Cục trưởng Cục Quản lý dược quyết định cấp giấy đăng ký lưu hành đối với hồ sơ đạt yêu cầu; Cục Quản lý dược có văn bản thông báo theo kết luận của Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc đối với hồ sơ thẩm định chưa đạt, không đạt và nêu rõ lý do.
Hiện nay, tại Việt Nam có 3 vaccine COVID-19 đang thử nghiệm lâm sàng ở các giai đoạn khác nhau. Trong đó, vaccine Nanocovax vừa hoàn tất tiêm thử nghiệm lâm sàng giai đoạn 3 trên 13.000 người tình nguyện tại Học viện Quân Y, tỉnh Hưng Yên và huyện Bến Lức, tỉnh Long An. Vaccine Covivac đang thử nghiệm lâm sàng giai đoạn 2 tại tỉnh Thái Bình với 375 người tình nguyện tham gia gồm hai nhóm đối tượng: nam và nữ, nhóm tuổi từ 18-59 và ≥ 60 tuổi. Vaccine ARCT-154 đang thử nghiệm lâm sàng giai đoạn đầu tiên tại Trường Đại học Y Hà Nội trên 100 tình nguyện viên. Người tình nguyện sẽ được tiêm hai mũi vaccine ARCT-154 hoặc giả dược cách nhau 28 ngày. Các dữ liệu an toàn sau tiêm mũi 1 (Ngày 1) đến 7 ngày sau tiêm mũi 2 (Ngày 36) sẽ được đánh giá.
P.V/TTXVN
-

-

-
-

-
 20/07/2025 05:55 0
20/07/2025 05:55 0 -
 20/07/2025 05:55 0
20/07/2025 05:55 0 -
 20/07/2025 05:52 0
20/07/2025 05:52 0 -
-

-
-
 20/07/2025 05:45 0
20/07/2025 05:45 0 -
 20/07/2025 05:45 0
20/07/2025 05:45 0 -
-
 19/07/2025 23:47 0
19/07/2025 23:47 0 -
 19/07/2025 23:47 0
19/07/2025 23:47 0 -
-

-

-

-
 19/07/2025 22:25 0
19/07/2025 22:25 0 - Xem thêm ›